- L'experiència de la làmina d'or
Per comprovar si el model de Thomson era cert, els científics Hans Geiger i Ernest Madsen, col.laboradors de Rutherford, van dissenyar una experiència aprofitant els últims descobriments de l'època sobre la radiació.
 |
| Font: slideshare.net |
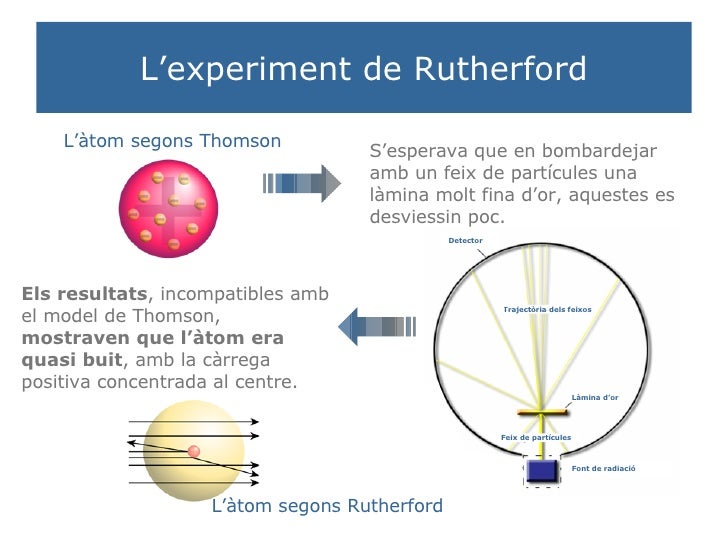
L'experiment consistia a llançar sobre una làmina molt prima d'or (només unes 1000 capes d'àtoms), un feix de partícules alfa.
El resultat va ser que pràcticament tot el feix de partícules alfa travessava la làmina d'or sense desviar-se, tal com s'esperaria.
Això no obstant, algunes partícules es desviaven considerablement i unes poques rebotaven i retrocedien.
L'unica explicació possible era que les partícules alfa hagueren xocat amb un nucli massiu i amb càrrega positiva. El fet que es desviaven molt poques, indicava que el nucli havia de tenir unes dimensions molt menudes amb relació a la grandària de l'àtom: es a dir, que practicament tot l'àtom era buit!
- El model de Rutherford
Amb els resultats anteriors, Rutherford va idear el model atòmic següent:
 |
| Font: Wikipedia |
L'àtom està format per un nucli molt menut i una escorça. Al nucli està concentrada tota la càrrega positiva i quasi tota la massa; a l'escorça es troben els electrons, que giren al voltant del nucli.
Per fer-nos-en una idea: si l'àtom fóra de la mida d'un camp de futbol, el nucli seria com una boleta col.locada al mig, i els electrons, com caps d'una agulla que girarien al voltant del camp.

